I. 서 론
철은 혈색소 생성에 중요한 물질로 주로 장내 흡수를 조절함으로써 철분의 체내 농도가 조절된다. 철을 배출하는 통로는 철이 포함된 장 상피 세포의 탈락이 유일하므로 철이 과도하게 체내에 축적되는 경우에는 심근, 간, 내분비계 등의 손상과 기능장애의 원인이 된다1.
철과잉증은 전신의 철 저장량 증가 및 그로 인한 조직손상과 장기부전으로 이어지는 다양한 상태이다. 1차성 철과잉증은 유전적 혈색소증에서 발생하며, 2차성 철과잉증은 일반적으로 잦은 수혈, 용혈, 철의 과도한 비경구적 또는 경구적 섭취, 만성 간질환 등으로 인해 발생한다2. 유전적 혈색소증은 한국을 비롯한 아시아 지역에서는 매우 드물어, 국내 철과잉증에 관한 연구는 골수형성이상증후군 또는 재생불량성빈혈 환자들이 만성적 수혈을 받게 됨에 따라 발생할 수 있는 수혈성 철과잉증 환자에 대한 증례 보고들이 대다수이다3.
철과잉증 환자 4명 중 3명은 보통 무증상이다. 철과잉증 관련 징후 및 증상이 나타나면 일반적으로 특정 장기 침범과 관련이 있다. 증상으로는 만성 피로, 관절통, 복통, 간비대, 심부전, 부정맥, 생식선기능저하증, 성욕 감퇴, 혈당 상승, 과색소침착(청동색 피부)을 보일 수 있다4.
체내에 과도하게 쌓인 철은 저절로 배출되지 않기 때문에 인위적으로 철을 배출해주어야 한다. 빈혈이 없는 경우 치료적 정맥절개술을 통해 철을 제거할 수 있으며, 대부분의 유전성 혈색소증에서 사용되고 있는 치료법이다. 치료적 정맥절개술을 받지 못하는 환자의 경우 철 킬레이트화 치료를 선택할 수 있다5.
진단은 혈청 페리틴 수치와 트랜스페린 포화도의 상승 소견으로 확인되며, 추가적으로 간기능검사, 유전자검사, 자기공명영상검사, 간 생검 등을 시행하여 페리틴 수치 상승의 원인 및 조직 내 철의 축적 여부를 확인할 수 있다. 혈청 페리틴 수치가 1000 ng/mL 이상일 경우 500 ng/mL씩 증가할 때마다 생존율은 약 30%씩 감소한다. 그러나, 조기에 진단하여 치료를 통해 철분 수치를 허용 가능한 수준까지 효과적으로 낮춘다면 그 예후는 매우 좋다. 혈청 페리틴 수치를 허용범위 내로 유지하는 환자에서 정상적인 수명 및 매우 낮은 간 손상 비율이 보고되었다6.
현재까지 철과잉증 환자에 대한 한방치료 증례논문이 보고되지 않았기에 철과잉증 환자에 대한 경험을 축적하는 것은 철과잉증에 대한 한방적 관리의 가능성을 더욱 확대할 수 있을 것으로 사료된다.
이에 본 증례는 혈색소증(철과잉증) 진단 후 1년 이상의 철 킬레이트화 치료에도 피로, 어지러움, 잦은 감기 및 구내염이 지속되어 철 킬레이트제 복용을 중단한 뒤 약 4개월간의 생간건비탕 복용기간 중 피로 증상의 호전과 혈청 페리틴 수치의 지속적인 개선을 확인하여 보고하는 바이다.
II. 증 례
본 증례는 경희대학교 한방병원 간장조혈내과에서 외래 치료 중인 철과잉증 환자 1명을 대상으로 한 후향적 증례보고로 경희대학교 한방병원 생명윤리위원회(Institutional Review Board, IRB)의 심의를 거쳤다(IRB Approval No. 2023-03-006).
1. 성별/연령 : 여성/56세
2. 내원기간 : 2022년 10월 31일~2023년 03월 15일
3. 주소증 : 피로감, 어지러움, 잦은 감기 및 구내염
4. 현병력
168 cm 48 kg 여성으로, 2017년 수회에 걸쳐 철분제 정맥주사를 받은 적 있으며, 2019년 건강검진 시 자기공명영상 검사상 간의 이상소견으로 □□대학교병원에 내원하여 혈색소증(Hemochromatosis) 진단받고 f/u하던 중 2021년 7월부터 2022년 10월 22일까지 엑스자이드필름코팅정(Deferasirox 90 mg)을 복용하였으며 철분 함량 높은 음식은 절제 중이었다. 철 킬레이트화 치료 중에도 피로감, 어지러움, 잦은 감기 및 구내염이 지속되어 철 킬레이트제 복용을 중단하고 2022년 10월 31일 ○○대학교 한방병원 한방내과 외래에 방문하였다.
5. 복약력
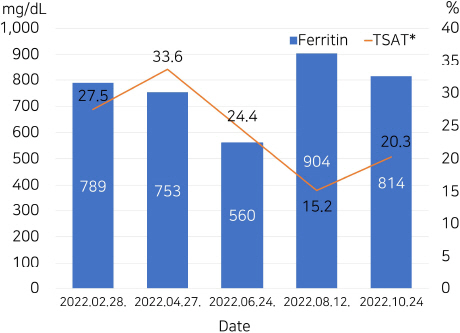
2021년 7월부터 엑스자이드필름코팅정(Deferasirox 90 mg, 철 킬레이트제)을 1일 1회 1정씩 복용하고 있었으며, 2022년 10월 22일부터 해당 약제 복용을 중단하였다. 약제 복용 중 □□대학교병원에서 시행한 철 표지자 검사는 Fig. 1과 같다.
Fig. 1
Changes in biochemical markers of iron status during deferasirox treatment.
TSAT* : Transferrin saturation (TSAT=Iron ÷TIBC×100), TIBC : total iron iron binding capacity, Reference value : Ferritin (9~89 ng/mL), TSAT (20~45%)
6. 과거력
1) 골다공증
2) 간의 이상소견 : 2019년 건강검진 시 자기공명영상 검사상 간의 이상소견이 확인되었다고 환자가 진술하였으나 검사 영상 및 판독 결과지를 지참하지 않아 확인할 수 없었다. 2020년 4월 3일 시행한 혈액검사 기록상 Aspartate Transaminase(이하 AST) 46 IU/L(0~35), Alanine Transaminase(이하 ALT) 39 IU/L (0~35)로 상승된 소견이 확인되었으며, AST와 ALT의 경도 상승 소견은 2021년 12월 3일까지 시행한 7회의 혈액검사 결과에서 지속되었다.
7. 가족력 : 父-당뇨병, 母-당뇨병
8. 내원 시 주요 검사 결과
1) 내원 시 지참한 혈액 검사 결과(2022년 10월 24일) : 백혈구 2.16×10^3/μl(4.0~10.0), 적혈구 4.06×10^6/μl(4.0~5.4), 혈색소치 12.0 g/dL(12~16), 적혈구용적률 36.7%(37~47), 혈소판 137×10^3/μl (150~350), 페리틴 814 ng/mL(13~150), 망상적혈구 1.42%(0.5~1.8)로 혈청 페리틴 수치의 상승 및 백혈구의 저하가 확인되었으며, PB smear 검사 상 Normocytic normochromatic RBCs, Moderate leukopenia with absolute neutropenia, Platelet is slightly decreased 소견이 확인되었다.
III. 연구방법 및 결과
1. 한방치료
환자는 2022년 11월 14일부터 2023년 03월 15일까지 본원에서 조제한 생간건비탕(生肝健脾湯) 2첩을 100 cc씩 3포로 전탕하여 매 저녁 식후 1~2시간에 100 cc씩 복용하였다. 약재 구성은 Table 1과 같다.
Table 1
Herbal Composition of Saenggangunbi-tang
2. 양방치료
2021년 7월부터 2022년 10월 22일까지 철 킬레이트제인 엑스자이드필름코팅정(Deferasirox 90 mg)을 1일 1회 1정씩 복용하였으며, 한방치료를 받는 기간(2022년 11월 14일부터 2023년 03월 15일)에는 엑스자이드필름코팅정을 복용하지 않았다.
IV. 고 찰
인체에는 과도한 철분을 배설할 수 있는 효과적인 방법이 없어 섭취한 철분에 대한 십이지장에서의 흡수 조절은 체내 철분 항상성에 중요한 역할을 한다. 인체는 하루에 1~2 mg의 식이 철을 흡수하며 이는 장세포와 피부상피세포 탈락이나, 월경 및 기타 혈액손실로 인한 철손실과 균형을 이룬다7. 흡수된 철의 대부분은 헤모글로빈 내에 저장되며 일부는 골수, 비장, 간에 저장된다. 전신 철 항상성 유지에는 세포 밖으로 철을 배출하는 수송체인 페로포틴(ferroportin)과 이를 조절하는 호르몬인 헵시딘(hepcidin)이 일차적으로 관여한다. 헵시딘은 주로 간에서 합성되며 장세포와 대식세포, 그리고 간세포 등에서 철이 혈장으로 유리되는 것을 방해하는 역할을 함으로써 혈중 철의 농도와 트랜스페린 포화도를 조절한다8.
철과잉증은 1차성 원인 및 2차성 원인에 의한 것으로 구분할 수 있다. 1차성 원인은 철흡수와 연관된 유전자의 이상에 의해 철과잉이 발생하는 경우로 유전적 혈색소증이 여기에 속한다. 2차성 원인에는 수혈, 용혈, 비경구적 또는 식이를 통한 철의 과도한 섭취 등이 있다6. 이전에는 혈색소증을 철과잉증과 혼용하며 원발성 혈색소증과 속발성 혈색소증으로 나누어 보는 경향이 있었으나, 2022년 International BioIron Society에서 각각의 정의와 분류가 확립되어 혈색소증은 철과잉을 유발할 수 있는 유전 질환들을 지칭하는 용어이며, 유전적 원인으로 인한 것이 아닌 철과잉은 더 이상 혈색소증으로 분류되지 않는다9.
철과잉증 진단 시 필요한 철 표지자는 대표적으로 혈청 페리틴 수치와 트랜스페린 포화도가 있다. 체내 저장 철의 양을 반영하는 페리틴 수치가 여성은 200 ng/mL 이상 남성은 300 ng/mL 이상, 트랜스페린 포화도가 여성은 45% 이상 남성은 50% 이상인 경우 철과잉을 시사한다10. 환자가 한방병원 내원 시 지참한 타병원 혈액검사 기록 상 혈청 페리틴 수치는 2022년 10월 24일 814 ng/mL으로 철과잉증 소견을 보였다.
본 증례 환자는 2019년 건강검진 시 자기공명영상 검사 상 간의 이상소견으로 방문한 □□대학교병원에서 혈색소증을 진단받았다. 그러나 혈색소증의 정의가 재정립되기 이전인 2019년에 진단을 받았던 점, 수회의 철분제 정맥투여 과거력, 유전적 혈색소증 진단을 위한 유전자 검사를 시행하지 않았던 점, 유전적 혈색소증은 한국을 비롯한 아시아 지역에서는 극히 드문 질환인 점을 고려하여 2019년도에 진단받았던 혈색소증은 2022년 International BioIron Society의 개정된 분류에 따라 과도한 철분제 투여로 인한 이차성 철과잉증으로 판단하였다.
철과잉증의 치료에 사용되는 철 킬레이트제는 인체 내 조직의 철과 결합하여 철분의 체외배출을 도와준다. 국내 철과잉증 치료 지침에 따르면 철 킬레이트제의 적절한 용량을 통해 혈청 페리틴을 1000 ng/mL 미만으로 유지하는 것을 목표로 한다11. 대표적 경구 철 킬레이트제인 Deferasirox의 일반적인 부작용으로는 복통, 메스꺼움, 구토, 설사, 요통, 피부 발진이 있으며 심하게는 위장관출혈, 신 독성, 간 독성의 부작용을 일으킬 수 있다12.
환자에게 투여한 생간건비탕은 인진오령산과 가감위령탕을 합하고 백작약, 육계, 반하 등을 제외한 처방이다. 간내 습열을 제거하고 이뇨, 건비(健脾), 안위(安胃), 이담(利膽)하는 효능이 있어 간기능을 개선하고 대사과정을 활성화하여 임상에서 생간건비탕을 투여하여 지방간, 간섬유화, 약인성 간손상 등의 다양한 간질환에 대한 개선 효과를 보인 사례들이 보고되고 있다13-15.
간은 당질대사, 단백질대사, 지질 및 콜레스테롤 대사 등의 영양 작용을 하며, 조혈 및 파혈작용을 하는 장기이다. 간은 철 대사에도 중요한 역할을 하는데, 간에서 합성되는 호르몬인 헵시딘은 장내 철 흡수를 조절함으로써 체내 철 수치를 조절하며 트랜스페린 및 세룰로플라스민과 같은 철분 대사의 주요 단백질 합성 부위이다16. 또한 간은 철분의 주요 저장 장소이며, 철분은 주로 페리틴 또는 헤모시데린의 형태로 간세포에 저장된다7. 철과잉 상태에서 자유 라디칼(free radical) 형성과 지질 과산화물(lipid peroxidation products)의 생성은 진행성 조직 손상을 초래하고 결국에는 간경화 또는 간세포암을 유발할 수 있다17.
내원 시 시행한 혈액검사 상 간기능의 이상소견은 확인되지 않았으나, 2019년 건강검진 시 자기공명영상 검사 상 간의 이상소견이 확인되었다는 환자의 과거력과 체내 철분대사 과정에서 간이 주된 역할을 하는 점을 고려하여 간의 대사과정을 활성화하고 간세포 보호 효과가 있어 제반 간질환에 광범위하게 사용되는 생간건비탕으로 철분 대사 활성 효과를 기대하였으며, 생간건비탕의 간 내 활성 산소 및 지질 과산화물 생성 억제효과18를 기대하여 철과잉으로 인한 간 조직 손상을 억제하고자 하였다.
본 증례 환자의 주호소 증상인 활동 시 피로감은 약 3개월 간의 한방치료 이후 상당히 호전되었다고 표현하였으며, 1개월 이후에도 호전상태로 유지 중이라고 하였다. 피로는 철과잉증의 흔한 증상으로, 철과잉증과 임상적 증상들의 관계를 분석한 연구19에서 피로의 간경화 및 간 내 철분 농도와의 관련성이 제시되었으나, 그 병인은 확실히 알려져 있지 않으며 부신피질자극호르몬분비호르몬의 이상과 관련이 있을 수 있다는 가설이 있다. 혈색소증 환자 169명에 대한 전향적 코호트 연구20결과에 따르면 피로는 철분 수치가 정상으로 회복된(de-ironed) 혈색소증 환자의 약 2/3 이상에서 일반적으로 확인되었고, 그 중 40%에서 피로 중증도가 다발성 경화증 또는 파킨슨병과 비슷한 정도(피로 심각도 척도 상 36점 초과)로 나타났다. 또한 해당 연구에서 피로는 혈청 페리틴 수치 또는 트랜스페린 포화도와 상관관계가 없는 것으로 보였다. 따라서 생간건비탕 복용 후 호전된 피로감은 혈청 페리틴 수치 저하와 함께 자연히 호전된 것이라고 보기에는 어렵다.
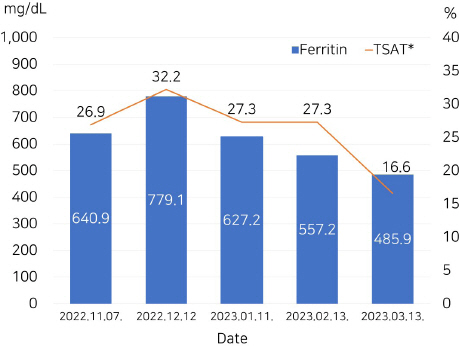
혈청 페리틴 수치는 2022년 11월 7일 640.9 ng/mL에서 약 4개월간의 한약치료 이후 2023년 3월 13일 485.9 ng/mL로 감소하였음을 확인할 수 있었으며, 간기능 검사 소견 또한 Alkaline phosphatase(ALP)의 경도 저하소견(28~29 U/L) 이외에는 치료기간 동안 참고치 내로 유지되어 간 독성의 부작용이 확인되지 않았다. 국내 철 킬레이트화 치료 지침11에 따르면 2회 연속 검사에서 혈청 페리틴 수치가 500 ng/mL 이하인 경우에는 철 킬레이트화 치료를 중단하고 혈청 페리틴 수치가 1000 ng/mL 이상으로 다시 증가하는 경우 다시 시작한다고 나와 있어, 환자의 혈청 페리틴 수치가 500 ng/mL 아래로 호전된 것은 임상적 의미가 있다. 생간건비탕 단독투여 후 관찰된 혈청 페리틴 수치 감소는 Deferasirox 경구 투여 시의 반감기가 8~16시간인 점을 고려하면 Deferasirox의 효과가 완전히 종료되었다고 판단된 시점에서의 결과이며, 과거 Deferasirox 복용기간 중 2개월 간격으로 측정한 혈청 페리틴 수치변화와 비교하였을 때 철 킬레이트화 치료 중단 후에도 페리틴 수치의 지속적인 호전을 보였다.
한편, 혈액검사 상 백혈구 수치가 내원 전부터 저하되어 있던 점을 확인할 수 있었으나 백혈구 수치는 생간건비탕 복용 전후로 큰 변화가 없었다. 또한 처음 내원 시 지참한 말초 혈액 도말검사 상 혈구의 형태학적 이상이 확인되지 않았고 혈액검사 상 백혈구 이외의 적혈구, 혈색소, 혈소판 수치가 참고치 내로 유지되고 있는 점을 통해 백혈구 저하의 원인을 특정할 수 없어, 혈액검사 추적관찰이 필요하다고 사료되었다.
본 증례는 이전까지의 국내 한방치료 보고가 부재한 철과잉증 환자에 대한 보고이며, 1년 이상의 철 킬레이트제 치료에도 피로, 어지러움, 잦은 감기 및 구내염이 지속되는 환자에게 생간건비탕을 투약하여 피로 증상의 호전을 확인하였다. 또한 철 킬레이트제 중단 후에도 생간건비탕 복용기간 중 페리틴 수치의 개선이 지속되었으며 간기능 검사 수치가 참고치 내로 유지되는 것을 확인하여 한방치료로 간손상 등의 부작용 없이 체내 철 과잉 상태 호전에 도움을 줄 수 있음을 보여주는 긍정적인 결과로 사료된다.
다만, 혈청 페리틴 수치는 염증, 감염 등의 상태에 영향을 받을 수 있고, 매일 수치에 변동이 있을 수 있으므로 철과잉증에 대한 생간건비탕의 명확한 치료효과 판정을 위해서는 추가적인 증례 관찰이 필요할 것으로 사료된다. 또한 객관적인 지표를 이용한 피로도의 평가가 이루어지지 않아 개선 정도를 명확히 확인하기 어려웠으나, 혈청 철 표지자 수치의 호전과 피로 증상의 개선이 비례하지 않는 경향이 있는 것으로 미루어 볼 때 한방 치료를 통해 철 킬레이트화 치료에도 지속되는 철과잉증 환자의 피로 개선에 좋은 치료가 될 수 있는 가능성을 보여준 것으로 생각된다.